✅ La tabla periódica revela propiedades, tendencias y relaciones entre elementos. Úsala para entender reactividad, masas y grupos químicos clave.
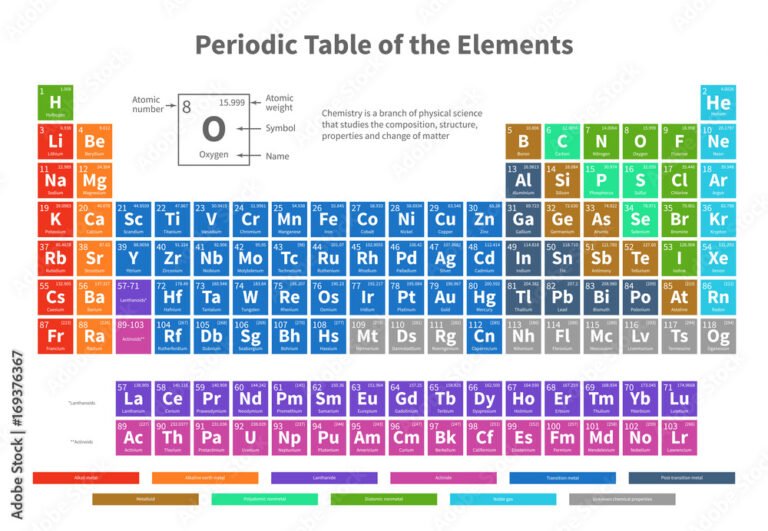
La tabla periódica es una herramienta fundamental para entender la naturaleza y propiedades de los elementos químicos. Utilizándola correctamente, se puede identificar fácilmente información clave como el número atómico, masa atómica, grupo, periodo y la familia a la que pertenece cada elemento, lo que facilita el estudio y la comprensión de su comportamiento químico.
En el siguiente artículo vamos a explorar cómo usar la tabla periódica para entender los elementos químicos, analizando su estructura y organización, además de explicar cómo interpretar los datos que nos brinda. También veremos ejemplos prácticos y consejos para que puedas aprovechar al máximo esta poderosa herramienta en tus estudios o trabajo.
¿Qué es la tabla periódica y cómo está organizada?
La tabla periódica es una representación ordenada de los elementos químicos conocidos, organizados en filas y columnas según sus propiedades y estructura atómica. Fue creada inicialmente por Dimitri Mendeléyev en 1869 y ha sido actualizada con el descubrimiento de nuevos elementos.
Filas o periodos
Las filas horizontales se denominan periodos. Cada periodo representa el número de niveles de energía que poseen los átomos de los elementos que contiene. A medida que avanzamos de izquierda a derecha en un periodo, aumentan el número atómico y las propiedades electrónicas.
Columnas o grupos
Las columnas verticales se llaman grupos. Los elementos dentro de un mismo grupo comparten similitudes en sus propiedades químicas porque tienen la misma cantidad de electrones en su capa de valencia. Por ejemplo, el grupo 1 contiene a los metales alcalinos, que son altamente reactivos.
Datos clave que aporta la tabla periódica para entender un elemento
- Número atómico (Z): Indica la cantidad de protones en el núcleo de un átomo, es único para cada elemento.
- Masa atómica: Representa el promedio ponderado de las masas de los isótopos del elemento.
- Símbolo químico: Abreviatura que representa al elemento, por ejemplo, H para hidrógeno o Fe para hierro.
- Estado de agregación: La tabla a veces indica si un elemento es sólido, líquido o gas a temperatura ambiente.
- Configuración electrónica: La tabla periódica, en combinación con conocimiento adicional, permite deducir la distribución de electrones y su nivel energético.
Cómo interpretar la posición de un elemento en la tabla periódica
La ubicación de un elemento en la tabla nos da pistas sobre su reactividad química y propiedades físicas:
- Metales, no metales y metaloides: Los metales se encuentran generalmente a la izquierda y en el centro de la tabla, los no metales a la derecha, y los metaloides indican características intermedias.
- Grupos con propiedades similares: Los elementos de un mismo grupo suelen compartir características químicas que determinan su uso y comportamiento.
- Tendencias periódicas: Propiedades como la electronegatividad, radio atómico, energía de ionización y afinidad electrónica varían de forma predecible a lo largo de la tabla, lo que ayuda a predecir cómo interactuarán unos elementos con otros.
Ejemplos prácticos para entender mejor la tabla periódica
Si analizamos el grupo 17 (halógenos), encontraremos elementos como flúor (F), cloro (Cl), bromo (Br) y yodo (I), que son muy reactivos y suelen formar sales con los metales. En cambio, los gases nobles situados en el grupo 18 son estables y poco reactivos debido a que tienen su capa de valencia completa.
Consejos para aprender a usar la tabla periódica
- Memorizar la ubicación de los grupos más relevantes y sus características principales.
- Observar las tendencias periódicas para predecir propiedades y reactividad.
- Practicar con ejercicios prácticos de identificación y clasificación de elementos según la tabla.
- Utilizar la tabla para entender combinaciones químicas básicas, como formación de compuestos y tipos de enlaces.
Análisis detallado de las tendencias periódicas y su influencia química
Cuando pensamos en la tabla periódica, no sólo visualizamos un conjunto de elementos, sino un mapa dinámico que revela patrones y tendencias fascinantes. Estas regularidades son las pistas que nos ayudan a predecir comportamientos, propiedades y reacciones químicas, transformando la tabla en una guía imprescindible para cualquier aficionado o profesional de la química.
Principales tendencias periódicas: la brújula del químico
- Radio atómico: El tamaño del núcleo atómico y su nube electrónica cambia sutilmente a lo largo de la tabla.
- Descenso por grupo: Al bajar en una columna, el radio aumenta por la incorporación de capas electrónicas.
- Avance por período: Al avanzar hacia la derecha, el radio disminuye por la mayor carga nuclear efectiva, atrayendo más fuerte a los electrones.
- Energía de ionización: La facilidad para quitar un electrón, crucial para entender reactividad.
- Tiende a incrementar al moverse hacia la derecha en un período.
- Disminuye al bajar en un grupo, ya que los electrones exteriores están menos ligados.
- Electronegatividad: La habilidad para atraer electrones durante un enlace químico.
- Generalmente aumenta a lo largo de un período.
- Disminuye descendiendo en un grupo.
¡Lo que estas tendencias nos dicen sobre los elementos!
| Propiedad | Tendencia | Influencia en la actividad química |
|---|---|---|
| Radio atómico | ⬆ bajando, ⬇ hacia la derecha | Define la reactividad y la formación de enlaces, ya que influye en cómo los átomos interactúan. |
| Energía de ionización | ⬇ bajando, ⬆ hacia la derecha | Un bajo valor facilita la pérdida de electrones, típico en metales; un alto valor indica estabilidad del electrón externo, común en no metales. |
| Electronegatividad | ⬇ bajando, ⬆ hacia la derecha | Determina la polaridad de los enlaces, clave para predecir propiedades moleculares y tipos de compuestos. |
Otras propiedades notables que no podés ignorar
- Afinidad electrónica: El gusto que tiene un átomo por adquirir electrones, una característica fundamental para comprender la formación de aniones.
- Electrones de valencia: Los protagonistas principales en las reacciones químicas, localizados en la capa más externa.
- Estado de oxidación: Indica la capacidad de un elemento para ganar o perder electrones durante reacciones químicas.
En definitiva, la tabla periódica es un verdadero libro abierto para quienes quieran sumergirse en el mundo de la química. Entendiendo estas tendencias, podés anticipar características y comportamientos que serían un misterio de otro modo.
Preguntas frecuentes
¿Qué información básica brinda la tabla periódica?
¿Cómo está organizada la tabla periódica?
¿Para qué sirve conocer los grupos de la tabla?
| Punto Clave | Descripción |
|---|---|
| Número atómico | Indica la cantidad de protones en el núcleo de un átomo. |
| Símbolo químico | Representa el elemento con una o dos letras. |
| Grupos | Columnas verticales que agrupan elementos con propiedades químicas similares. |
| Periodos | Filas horizontales que ordenan elementos por nivel de energía y número atómico. |
| Metales, no metales y metaloides | Clasificación según propiedades físicas y químicas. |
| Elementos representativos | Grupos 1, 2 y del 13 al 18, con propiedades variadas y representativas. |
| Elementos de transición | Grupos 3 al 12, suelen ser metales con alta conductividad. |
| Propiedades periódicas | Tendencias como electronegatividad, radio atómico y energía de ionización. |
| Uso en química | Permite predecir comportamientos y reacciones químicas. |
Te invitamos a dejar tus comentarios abajo y a revisar otros artículos de nuestra web que podrían interesarte, como «Los tipos de enlaces químicos» y «Cómo interpretar las reacciones químicas.»