✅ Número atómico indica protones, define elemento; número másico suma protones y neutrones, da masa del núcleo. ¡Clave en química y física!
La diferencia entre número atómico y número másico radica en los componentes del átomo a los que hacen referencia: el número atómico indica la cantidad de protones en el núcleo de un átomo, mientras que el número másico representa la suma total de protones y neutrones que posee dicho núcleo. Entender esta distinción es fundamental para comprender cómo se clasifican los elementos y sus isotopos dentro de la tabla periódica.
A continuación, profundizaremos en la definición de cada uno, explicaremos su importancia en la química y la física, y veremos ejemplos concretos para clarificar estas diferencias esenciales en el estudio de la materia. Además, exploraremos cómo estos números se expresan y utilizan en la notación atómica.
Definición de Número Atómico
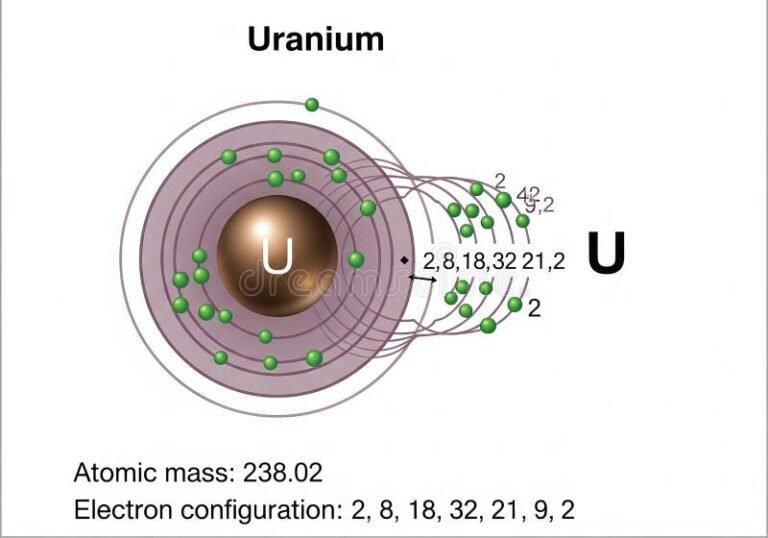
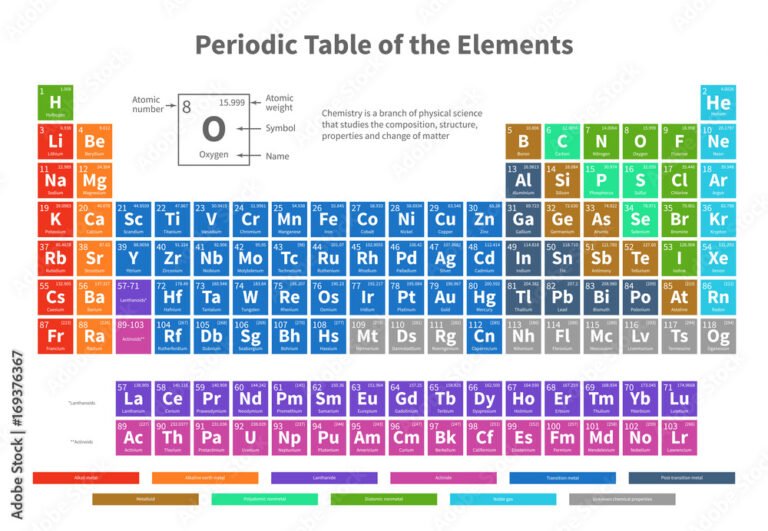
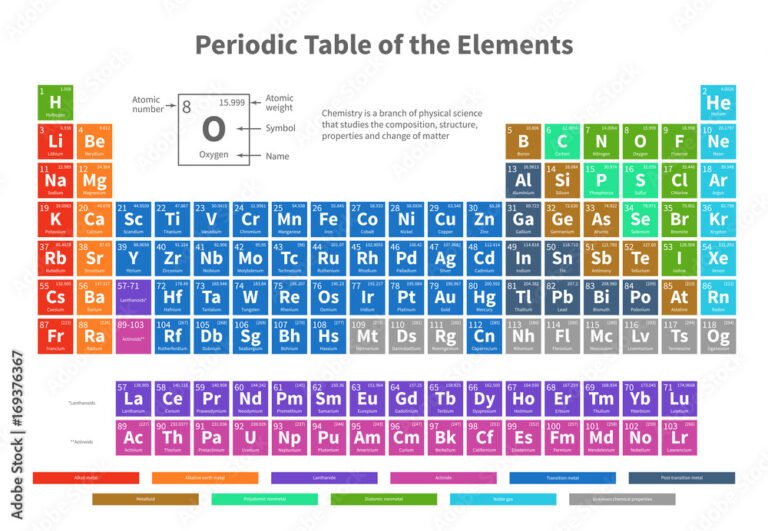
El número atómico, representado comúnmente por la letra Z, es el número de protones que se encuentran en el núcleo del átomo. Este número es único para cada elemento químico y determina su identidad y posición en la tabla periódica. Por ejemplo, el número atómico del carbono es 6, lo que significa que todo átomo de carbono tiene 6 protones en su núcleo.
Importancia del Número Atómico
- Identifica el elemento: Cada elemento tiene un número atómico diferente.
- Determina el comportamiento químico: El número de protones afecta directamente las propiedades químicas y la configuración electrónica del átomo.
- Número de electrones en un átomo neutro: En un átomo sin carga, la cantidad de electrones es igual al número de protones.
Definición de Número Másico
El número másico, indicado por la letra A, es la suma total de protones y neutrones en el núcleo de un átomo. Los neutrones no tienen carga eléctrica, pero su presencia afecta la masa del núcleo y puede influir en la estabilidad del átomo. Por ejemplo, el carbono más común tiene un número másico de 12 (6 protones + 6 neutrones), aunque existen isótopos con diferente número másico.
Importancia del Número Másico
- Indica la masa atómica aproximada: Aunque la masa total del átomo también depende de otros factores, el número másico es una buena aproximación de su masa.
- Identifica isótopos: Átomos del mismo elemento (igual número atómico) que tienen diferente número másico debido a distintas cantidades de neutrones son llamados isótopos.
- Afecta la estabilidad nuclear: La proporción de neutrones y protones influye en la capacidad del núcleo para permanecer estable o radioactivo.
Diferencias Clave entre Número Atómico y Número Másico
| Categoría | Número Atómico (Z) | Número Másico (A) |
|---|---|---|
| Definición | Número de protones en el núcleo | Suma de protones y neutrones en el núcleo |
| Elemento Químico | Determina el elemento | No determina el elemento, sino el isótopo |
| Uso | Identificar y ordenar elementos en la tabla periódica | Identificar isótopos y masa aproximada del átomo |
| Valor | Siempre un número entero | Generalmente un número entero, pero puede variar según isótopos |
Ejemplo Práctico: El Carbono
Veamos el caso del carbono para entenderlo mejor:
- Número atómico (Z): 6 – Esto indica que todo átomo de carbono tiene 6 protones.
- Número másico (A): El carbono más común es el carbono-12 con 6 protones y 6 neutrones, por lo que su número másico es 12.
- También existe el carbono-14, un isótopo radiactivo con 6 protones y 8 neutrones, por lo que su número másico es 14.
Con esta explicación, queda claro que mientras el número atómico define la identidad del elemento químico, el número másico proporciona información sobre la masa y la versión isotópica del átomo.
Aplicaciones Prácticas del Número Atómico y Másico en Química y Física
En el fascinante mundo de la química y la física nuclear, entender el número atómico y el número másico no es solo un tema de memorizar conceptos, sino que es clave para múltiples aplicaciones prácticas que impactan desde la identificación de elementos hasta la generación de energía. Veamos cómo estos dos valores se ponen en acción.
¿Para qué sirve el número atómico?
El número atómico (Z) no es simplemente un número; es el código de identidad de cada elemento en la tabla periódica. Algunas de sus aplicaciones más relevantes son:
- Clasificación de elementos: El número atómico determina la posición exacta del elemento, definiendo su comportamiento químico y propiedades periódicas.
- Identificación de isótopos: Aunque los isótopos tienen el mismo Z, es fundamental conocer este número para diferenciarlos junto con el número másico.
- Diseño y análisis de reacciones químicas: Conocer la cantidad de protones ayuda a prever la formación de iones y compuestos.
El número másico como herramienta en física y química ⚛️
El número másico (A) ofrece información sobre la masa y la estabilidad del núcleo atómico:
- Determinación de isótopos:
- Isótopos son átomos del mismo elemento (igual Z) pero con diferente A.
- Implica variaciones en las propiedades nucleares, desde la estabilidad hasta la radioactividad.
- Aplicaciones en datación radiométrica:
- El conocimiento del número másico permite precisar la edad de materiales mediante el análisis de isótopos.
- Reacciones nucleares y energía:
- El cálculo de número másico es fundamental para diseñar reactores nucleares y comprender la fisión y fusión.
Tabla comparativa: Número Atómico vs Número Másico
| Aspecto | Número Atómico (Z) | Número Másico (A) |
|---|---|---|
| Definición | Cantidad de protones en el núcleo | Suma de protones y neutrones en el núcleo |
| Determina | La identidad y posición del elemento | El isótopo y la masa atómica |
| Unidad | Sin unidad (número entero) | Unidades de masa atómica (uma) para masa real |
| Importancia en | Química, tabla periódica, reactividad | Física nuclear, estabilidad, radioactividad |
¿Querés un ejemplo para entender mejor?
Tomemos el caso del carbono, para entender cómo estos números impactan en la vida real.
- Carbono-12: Z = 6, A = 12. Es el isótopo más abundante y estable.
- Carbono-14: Z = 6, A = 14. Radiactivo, utilizado para datar materiales orgánicos.
Así, estos números no sólo son datos abstractos sino herramientas que hacen posible desde conocer la composición de un objeto hasta medir la antigüedad de fósiles, o incluso, controlar procesos energéticos en centrales nucleares.
Preguntas frecuentes
¿Qué indica el número atómico?
¿Qué representa el número másico?
¿Puede cambiar el número atómico en un elemento?
| Punto Clave | Descripción |
|---|---|
| Número Atómico (Z) | Cantidad de protones en el núcleo, identifica el elemento químico. |
| Número Másico (A) | Suma de protones y neutrones en el núcleo del átomo. |
| Isótopos | Átomos del mismo elemento con distinto número másico por diferente cantidad de neutrones. |
| Simbolización del elemento | Se representa como _{Z}^{A}X, donde X es el símbolo químico. |
| Importancia del número atómico | Determina propiedades químicas y posición en la tabla periódica. |
| Variabilidad del número másico | Puede variar entre átomos del mismo elemento formando isótopos. |
| Protones | Carga positiva, igual al número atómico. |
| Neutrones | Sin carga eléctrica, afectan la estabilidad y masa del átomo. |
| Masa atómica promedio | Promedio ponderado de todos los isótopos del elemento. |
Dejá tus comentarios y no olvides revisar otros artículos de nuestra web que seguro te van a interesar.