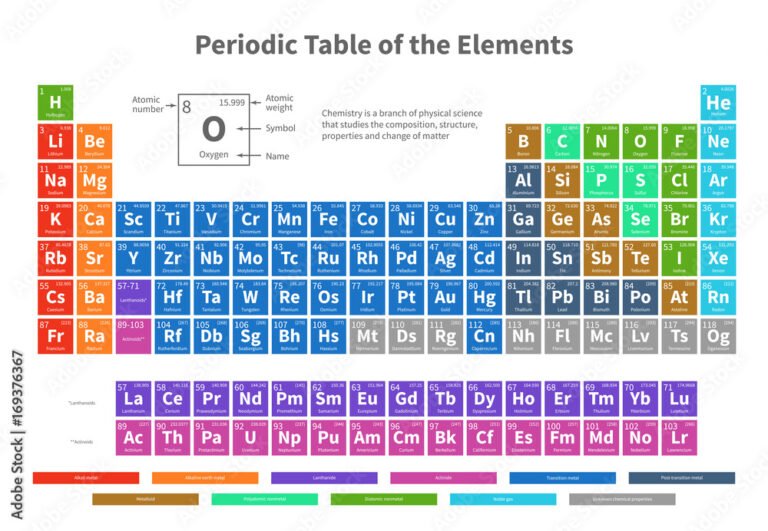
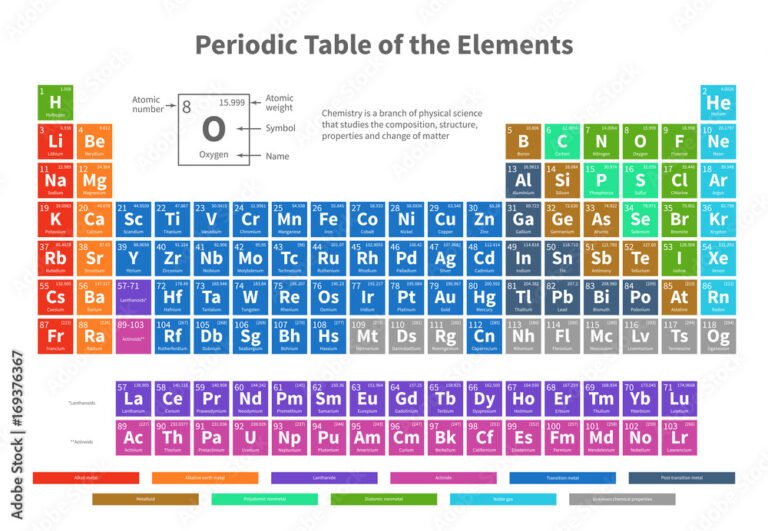
✅ Los grupos y períodos de la tabla periódica organizan elementos según propiedades químicas y electrónicas, clave para entender reacciones y comportamiento atómico.
Los grupos y periodos de la tabla periódica son las formas en que se organizan los elementos químicos para facilitar su estudio y comprensión. Los grupos son las columnas verticales, mientras que los periodos son las filas horizontales. Esta organización permite predecir las propiedades químicas y físicas de los elementos, así como entender sus relaciones y comportamientos.
En este artículo te explicaremos en detalle qué son exactamente los grupos y periodos en la tabla periódica, cómo se clasifican y cuáles son sus aplicaciones prácticas más importantes. Entender esta estructura es clave para estudiantes, científicos y cualquier persona interesada en la química, ya que proporciona una herramienta fundamental para analizar la materia y sus transformaciones.
¿Qué Son Los Grupos En La Tabla Periódica?
Los grupos son las columnas verticales de la tabla periódica y están numerados del 1 al 18 siguiendo la IUPAC (Unión Internacional de Química Pura y Aplicada). Cada grupo agrupa a los elementos que tienen las mismas propiedades químicas y el mismo número de electrones en su capa externa, llamados electrones de valencia.
Características de los Grupos
- Elementos con comportamiento químico similar: Por ejemplo, todos los elementos del grupo 1 (los alcalinos) reaccionan violentamente con el agua.
- Estado de oxidación común: Generalmente comparten un mismo estado de oxidación.
- Electron Configuration: La configuración electrónica externa es similar dentro de un grupo.
Ejemplos de Grupos Importantes
- Grupo 1 – Metales Alcalinos: Litio (Li), Sodio (Na), Potasio (K), etc.
- Grupo 17 – Halógenos: Flúor (F), Cloro (Cl), Bromo (Br), etc.
- Grupo 18 – Gases Nobles: Helio (He), Neón (Ne), Argón (Ar), etc.
¿Qué Son Los Periodos En La Tabla Periódica?
Los periodos son las filas horizontales de la tabla periódica. En total hay 7 períodos, que indican la cantidad de niveles de energía o capas electrónicas que tienen los átomos de los elementos que los componen.
Características de los Periodos
- Nivel de energía: Cada período indica un nivel energético diferente donde se ubican los electrones.
- Propiedades variables: Las propiedades cambian progresivamente de un extremo a otro a lo largo de un período.
- Aumento del número atómico: Al avanzar en un período, el número atómico (cantidad de protones) incrementa de manera consecutiva.
¿Para Qué Sirven Los Grupos Y Periodos?
La organización en grupos y períodos permite:
- Predecir propiedades químicas y físicas: Saber el comportamiento típico de un elemento basándose en su posición.
- Facilitar el aprendizaje y la clasificación: Agrupar elementos con características similares para estudiarlos en conjunto.
- Entender la estructura atómica: Relacionar la tabla con la configuración electrónica.
- Aplicaciones prácticas: Desde la química industrial hasta la medicina, se utiliza para seleccionar materiales o entender reacciones.
Ejemplos de Uso Práctico
Por ejemplo, si queremos saber qué metal es más reactivo o apto para construir un electrodo, podemos mirar en el grupo 1. Si se busca un gas inerte para un experimento, elegiremos dentro del grupo 18.
Resumen de la Estructura de La Tabla Periódica
| Aspecto | Grupos | Periodos |
|---|---|---|
| Dirección | Vertical (Columnas) | Horizontal (Filas) |
| Número Total | 18 | 7 |
| Qué indica | Electrones de valencia y propiedades químicas similares | Nivel de energía y número atómico creciente |
| Ejemplo | Grupo 1: Metales alcalinos | Periodo 2: elementos como Carbono y Nitrógeno |
Análisis detallado de la configuración electrónica asociada a grupos y periodos
Cuando hablamos de la configuración electrónica, nos metemos en el corazón mismo de la estructura atómica que define a cada elemento. Entender cómo se distribuyen los electrones en sus niveles y subniveles es la clave para comprender por qué los grupos y periodos en la tabla periódica se comportan de determinada manera.
La base: niveles y subniveles electrónicos
Antes de saltar a la mesa completa, veamos cómo se organizan los electrones:
- Niveles de energía (capas): Representados por números enteros (1, 2, 3…), que corresponden a las órbitas alrededor del núcleo.
- Subniveles: Dividen a cada nivel y se identifican como s, p, d y f, con diferente capacidad máxima de electrones.
Capacidad máxima por subnivel
| Subnivel | Electrones máximos |
|---|---|
| s | 2 |
| p | 6 |
| d | 10 |
| f | 14 |
¿Cómo se relaciona todo esto con los grupos y periodos?
- Periodos: Cada periodo corresponde a un nivel de energía principal. Por ejemplo, el primer periodo tiene electrones en el nivel 1, el segundo en el nivel 2, y así sucesivamente.
- Grupos: Los elementos en un mismo grupo suelen terminar la configuración electrónica con el mismo tipo y número de electrones en el subnivel más externo, lo que los hace tener propiedades químicas similares.
Ejemplificando: configuración electrónica del sodio (Na) y potasio (K)
- Sodio (Na): 1s² 2s² 2p⁶ 3s¹ — pertenece al grupo 1, tiene 1 electrón en su subnivel s más externo del tercer nivel.
- Potasio (K): 1s² 2s² 2p⁶ 3s² 3p⁶ 4s¹ — también grupo 1, este electrón valente está en el nivel 4, subnivel s.
Esto explica por qué ambos son tan salados y hacen patinar a la tabla química: comparten comportamiento por esa gran estrella, el electrón valente.
Otros aspectos interesantes
- Electrones de valencia y reactividad: Los electrones en el último nivel energético determinan cómo interactúa un átomo con otros, y por ende su reactividad química.
- Configuraciones atípicas: Algunos elementos en el bloque d y f tienen excepciones a la «regla» general debido a factores de estabilidad.
Preguntas frecuentes
¿Qué es un grupo en la tabla periódica?
¿Qué significa un periodo en la tabla periódica?
¿Para qué sirven los grupos y periodos?
| Punto Clave | Descripción |
|---|---|
| Grupos | Son 18 columnas verticales que organizan elementos según propiedades químicas semejantes. |
| Periodos | Son 7 filas horizontales que indican la cantidad de niveles de energía de los átomos. |
| Elementos Representativos | Incluyen los grupos 1, 2 y del 13 al 18, con propiedades químicas variadas. |
| Elementos de Transición | Ubicados en los grupos 3 al 12, con electrones en orbitales d. |
| Elementos de Transición Interna | Comprenden lantánidos y actínidos, con electrones en orbitales f. |
| Configuración Electrónica | Se relaciona con la posición en grupo y periodo, indicando comportamiento químico. |
| Propiedades periódicas | Tales como radio atómico, electronegatividad, varían según grupos y periodos. |
| Uso práctico | Facilita la predicción de reactividad y propiedades físicas de los elementos. |
Te invitamos a dejar tus comentarios abajo y a revisar otros artículos de nuestra web para aprender más sobre química y ciencia en general.